Prevence demence a poruchy paměti

Proces stárnutí našeho mozku, během něhož dochází přirozeně k poklesu kognitivního výkonu, je také definován jako kognitivní stárnutí.
Jakými změnami mozku je tento proces provázen? A lze z vědeckého, lékařského a psychologického hlediska tento proces ovlivnit?
Odborníci se na základě vědeckého výzkumu shodli na názoru, že pokud mozku dodáváme pravidelně látku cholin v co nejpřirozenější formě, pak náš mozek nejen stimuluje, ale dokonce i pomáhá přenášet nervové vzruchy v mozku, tím se zlepšuje naše paměť a kognitivní funkce.
Jejím pravidelným podáváním se také prokazatelně snižuje riziko degenerativních postižení mozku, jako jsou demence, Alzheimerova choroba nebo Parkinsonova nemoc.
Kromě lékařských studií je zde ještě aspekt subjektivního vnímání pocitu klienta, který se po pravidelném užívání doplňku s obsahem cholinu cítí svěže, má více energie, zaznamenává zvýšenou pozornost a koncentraci. U svých klientů v poradenské praxi se setkávám s klienty s degenerativním postižením mozku. Kromě klasické medikace určené neurologem dochází u nich pravidelným podáváním tohoto doplňku jak ke zlepšení klinického stavu, tak i psychické a sociální pohody. Podle mých praktických zkušeností se klientovi po čase vrací opět kvalita sociálního života, samozřejmě s ohledem na aktuální klinický obraz.
- Kognitivní funkce mohou být postiženy různou měrou a různým způsobem.
V běžném procesu stárnutí dochází přirozeně k postupnému zapamatování a uložení se do paměti, ale paměťová stopa se buď nevytvoří, nebo jen na krátkou dobu a velmi rychle zaniká. Potíže s vybavováním si vjemů je dalším příkladem kognitivního stárnutí. Z vědeckého a lékařského hlediska je nejdůležitější objev acetylcholinu – jako prvního neurotransmitéru – neuropřenašeče. Byl objeven Henrym Halletem Dalem v roce 1914, jeho úkolem je generovat podněty v částech nervového systému – působí jako posel a přenašeč.
Nejčastější poruchou paměti je demence. Změny kognitivních funkcí mohou mít výrazný odraz v somatickém stavu nemocného a mohou významným způsobem ovlivňovat celkový zdravotní stav organismu. Demence neurodegenerativního původu – Alzheimerova choroba – je nejčastější příčinou demencí vůbec. Je zodpovědná minimálně za 60 % demencí, z nichž některé jsou spolupodmíněny účastí vaskulární složky (smíšené demence). Alzheimerova choroba má specifický neuropatologický obraz. Z transmembránového neuronálního proteinu, amyloidového prekurzorového proteinu jsou působením enzymů beta- a gama-sekretáz extracelulárně odštěpovány peptidy o délce 40–42 aminokyselin (u zdravých lidí jsou odštěpovány kratší fyziologické fragmenty za účasti enzymu alfa-sekretázy). Postižené neurony podléhají apoptóze a zanikají. Makroskopicky dochází k mozkové atrofii, která začíná v meziální temporální oblasti – nejdříve postihuje hipokampy, dále amygdaly a čichový kortex. Postupně atrofují temporální a parietální laloky. Frontální a okcipitální laloky atrofují podstatně méně.
Z neurotransmiterových systémů je u Alzheimerovy choroby porušen již v časném stadiu centrální acetylcholinergní systém. Toto je další důvod k doplňování látky cholinu s dalšími na sebe navazujícími prvky.
- Teoretická východiska a fyziognomie:
Případové kvalitativní a kvantitavní vědecké studie týkající se pozitivního působení cholinu na kognitivní funkce mozku se stále vyvíjí. Naším úkolem jako odborníků z řad lékařských a psychologických je informovat kromě vědecké obce také širokou veřejnost.
Mezi důležitými složkami kognitivních funkcí jsou paměť a schopnost učení se.
Paměť lze dělit podle více typů různých hledisek. Jedním z nich je dělení podle časové následnosti na paměť ultrakrátkou (ikonickou, echoickou, vyžadující správnou funkci frontálních laloků), krátkodobou (je realizována dočasnými nervovými spoji, dočasně vzniklými reverberačními okruhy; účastní se jí především hipokampy a při vybavení frontální laloky) a v procesu konsolidace vznikající dlouhodobou paměť (vytvoření paměťových engramů – syntéza specifických bílkovin, změny neuronálních dendritů – ke vzniku je třeba mechanizmu dlouhodobé potenciace probíhající na N-metyl-D-aspartátových (NMDA) glutamátergních receptorech s následnou aktivací některých proteinkináz i dalších enzymů – probíhá v hipokampu, ukládá se v různých oblastech neokortexu, k vybavení je třeba frontální lalok).
Dlouhodobá paměť je dělena do dvou skupin na deklarativní a nedeklarativní.
Deklarativní paměť – obsahy této paměti jsou přístupné vědomému vybavení, lze je vyjádřit slovy. Deklarativní paměť vyžaduje funkci hipokampů.
Epizodická paměť bývá porušena např. u Alzheimerovy choroby nebo Korsakovova syndromu, sémantická např. u subtypu frontotemporální lobární degenerace.
Nedeklarativní paměť je implicitní, není přístupna vědomému vybavení. Patří sem např. podmíněné reflexy, emoční paměť, habituace, senzitizace, důležitou složkou je tzv. procedurální paměť, ve které jsou uloženy naučené motorické dovednosti, jako jsou řeč, chůze apod. Nedeklarativní paměť nezávisí na funkci hipokampů, ale na funkci bazálních ganglií, cerebella a neokortexu. Jako příklad postižení mohou sloužit tzv. podkorové (subkortikální) demence, např. demence u Parkinsonovy choroby.
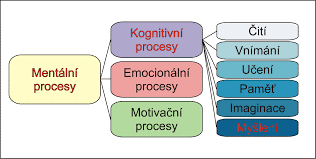
Zdroj: https://pfyziolmysl.upol.cz/?p=1662
- Kazuistika z praxe psychologa
Ve své praxi poradenského psychologa se setkávám s pacienty, kteří trpí poruchou paměti nebo degenerativním postižením mozku.
Jejich problémem je snížená funkce udržení různých informací v paměti delší dobu, což je pro ně velmi stresující. Demence takto velmi úzce souvisí i s následnou depresí, protože neschopnost uchovat si v krátkodobé paměti základní informaci je frustrující jak pro pacienty samotné, tak i pro jejich okolí.
Většinou dochází v rodinách s těmito pacienty k narušení sociálních vazeb a vztahů. Ne každý má trpělivost s pacientem s demencí. Vznikají tak na pacienta tlaky, nakonec může dojít i k jeho sociální izolaci, kdy ho přátelé a rodinní příslušníci úplně přestanou navštěvovat.
Sekundární deprese ze sociální izolace je nejčastějším dalším přidaným symptomem k diagnóze pacienta s demencí. A přitom by stačilo využít podporu a vstřebávání cholinu v mozku dodáváním této látky.
Klientka Petra, 58 let, Praha – žije s manželem v rodinném domě, její diagnóza je Alzheimerova choroba – 1. stadium. Projevuje se u ní častým zapomínáním, ulpíváním na jedné myšlence a zacyklením se na ní. V tomto stadiu dokáže klientka ještě samostatně fungovat, je schopna základní obsluhy, dojít na malý nákup a uklidit domácnost. Bohužel ale už nezvládne zapamatovat si data a události na sebe kontinuálně navazující. Po pravidelném podávání cholinu a další indikované medikace od neurologa se její paměť dostala do fáze, kdy se zpomalilo stadium dalšího zapomínání – je schopna si udržet v krátkodobé paměti důležité události a je schopna poznat rodinné příslušníky. Před pravidelným užíváním cholinu měla stavy, kdy volala dceři, že je doma cizí pán – ve skutečnosti to byl její manžel, jehož nepoznávala. Její zdravotní stav je nyní stabilizován a upravily se i sociální vazby v rodině.
Klíčová slova:
kognitivní změny ve stáří, kognitivní funkce, poruchy paměti, ovlivnitelné poruchy paměti, testování kognitivních funkcí
Použitá literatura:
https://pfyziolmysl.upol.cz/?p=1662
https://slideplayer.cz/slide/12111767/
1. Ambler Z., Bednařík J., Růžička E. a kol. Klinická neurologie, část obecná. Praha: Triton, 2004.
2. Bartoš A. Zjevná afázie není přítomna ani ve středním stadiu Alzheimerovy nemoci. Cesk Slov Ne urol N 2010; 3: 254–257.
3. Bartoš A., Hasalíková M. Poznejte demenci správně a včas – příručka pro klinickou praxi. Praha: Mladá fronta 2010.
4. Bartoš A., Píchová R., Trojanová H., Lang O., Řípová D. SPECT mozku v diagnostice Alzheimerovy nemoci. Psychiatrie 2008; 12 (Supll 3): 8–11. 77 www.neurologiepropraxi.cz | 2012; 13(2) | Neurologie pro praxi Hlavní téma
5. Bartoš A., Zach P., Tintěra J., Ibrahim I., Řípová D. Jednoduchá klasifikace změn bílé hmoty na MR mozku ve stáří. Psychiatrie 2010; 14 (Suppl 2): 44–47.
6. Budson A. E., Solomon P. R. Memory loss. A practical guide for clinicians. Elsevier Sounders, 2011.
7. Hort J., Rusina R. a kol. Paměť a její poruchy – paměť z hlediska neurovědního a klinického. Praha: Maxdorf, 2007.
8. Jirák R., Koukolík F. Demence. Neurobiologie, klinický obraz, terapie. Praha: Galén, 2004.
9. Kopeček M. Psychomtorické tempo, rychlost řeči a myšlení. Psychiat. pro praxi, 2007; 8(5): 213–215.
10. Košťálová M., Bednařík J., Skutilová S., Mitášová A., Bártková E., Šajgalíková K., Demovičová A., Dušek L. Afázie a její vztah k tíži kognitivního deficitu u demence. Cesk Slov Neurol N 2010; 73/106(3): 258–266.
11. Levine P. A., Langa KM. Vascular cognitive impairment: disease mechanisms and therapeutic implications. Neurotherapeutics. 2011; 8(3): 361–373.
12. Moorhouse P., Rockwood K. Vascular cognitive impairment: current concepts and clinical developments. Lancet Neurol. 2008; 7(3): 246–255.
13. Musil L., Bartoš A., Matěj R., Elleder M., Hřebíček M. Unusual cause of stroke: CADASIL with novel mutation in Czech patient. Čes a slov Neurol Neurochir 2006; 69/102(4): 311–314.
14. Rektorová I. et al. Kognitivní poruchy a demence. Praha: Triton, 2007.
15. Rektorová I. Neurodegenerativní demence. Cesk Slov Neurol N 2009; 72/105: 97–109.
16. Ressner P., Hort J., Rektorová I., Bartoš A., Rusina R., Línek V., Sheardová K. Doporučené postupy pro diagnostiku Alzheimerovy nemoci a dalších onemocnění spojených s demencí. Cesk Slov Neurol N 2008; 71/104(4): 494–501.
17. Rusina R., Matěj R. Vaskulární demence. Psychiat. praxi; 2007; 2: 81–84.
18. Růžička E., et al. Diferenciální diagnostika a léčba demencí. Příručka pro praxi. Praha: Galén, 2003. 19. Sheardová K., Hort J., Rusina R., Bartoš A., Línek V., Ressner P., Rektorová I. Doporučené postupy pro léčbu Alzheimerovy nemoci a dalších onemocnění spojených s demencí. Cesk Slov Neurol N 2007; 70/103(5): 589–594.

